Какое физическое явление лежит в основе работы однофотонного эмиссионного компьютерного томографа
Обновлено: 06.07.2024
Эмиссионная компьютерная томография (ЭКТ) позволяет получать послойные распределения функциональных характеристик в биотканях, не учитывающие вклад радиоактивности от выше- и нижележащих слоев исследуемого органа. Метод ЭКТ рассматривается в двух независимых вариантах. Это однофотонная эмиссионная компьютерная томография(ОФЭКТ), основанная на применении радиоизотопов типа 99 Те, испускающих одни гамма-квант при распаде ядра, и позитронная эмиссионная томография(ПЭТ), использующая радиоизотопы типа 68 Ga. ЭКТ изображения, харак-щие физиологические и метаболические процессы в организме, имеют пространственное разрешение порядка 15-20 мм в ОФЭКТ-системах, что хуже систем ТКТ(1мм). Но чувствительность обнаружения при использовании ОФЭКТ и ПЭТ значительно выше чувствительности обнаружения при использовании структурных методов, кроме того, ОФЭКТ и ПЭТ позволяют определять пикомолярные и наномолярные концентрации меченых веществ. Наиболее часто используемый прибор для однофотонной эмиссионной компьютерной томографии – это стандартная гамма-камера, изобретенная Ангером в середине прошлого века.
Однофотонный эмиссионный компьютерный томограф состоит из следующих основных состав-

Принцип однофотонной эмиссионной компьютерной томографии заключается в получении серии сцинтиграмм при программно-управляемом вращении одного или нескольких детекторов томографа вокруг продольной оси тела пациента, которому введен необходимый для исследования РФП. Проекции изображения, полученные за полный оборот детекторной системы, обрабатываются компьютером, и по специальным алгоритмам производится реконструкция аксиальных, коронарных, сагиттальных и косых срезов.
Без выполнения ряда следующих требований невозможно рассчитывать на получение высоко-
качественных томографических изображений. 1. Детектирующая система должна иметь высокую стабильность, однородность и пространственную линейность поля. Наличие микропроцессоров,
которые в реальном масштабе времени проводят автоподстройку параметров, сводит к минимуму
влияние артефактов. 2. Важным требованием является качество штативно-поворотного устройства и ложа для пациента. 3. Система должна иметь современный мощный компьютер с программами контроля качества, реконструкции изображений, обработки и отображения информации.
Для получения качественного изображения необходимо учитывать следующие параметры:
1). Активность РФП, вводимых пациенту. Чем больше эта активность, тем меньше время исследования и более высока статистическая достоверность информации. Но при этом увеличивается лучевая нагрузка на организм пациента и на персонал. 2). Размерность матрицы сбора информации рассчитывается как отношение размера детектора к размеру пиксела. В свою очередь размер пиксела определяется величиной необходимого разрешения и равен половине или трети разрешения. На практике чаще всего используют матрицу размерности 64×64 пиксела. Для повышения разрешающей способности сбор информации желательно проводить на матрицу размерности 128×128 пикселов. Но при этом: увеличивается время регистрации исходной
информации; уменьшается количество импульсов на одну проекцию (уменьшается статистическая достоверность информации); увеличивается время реконструкции срезов;
информация занимает много памяти на магнитных или оптических дисках; для обеспечения статистической достоверности информации и сокращения времени исследования необходимо вводить большую активность РФП. Поэтому матрицу размерности 128×128 пикселов используют преимущественно при работе на двух- или трех детекторных томографах, оснащенных современными компьютерами.3). Число проекций изображения. В идеале расстояние, которое проходит детектор томографа между проекциями, равняется величине размера матричного пиксела. Поэтому число проекций изображения определяется отношением длины окружности или эллипса к размеру пиксела. Вообще здесь действует принцип — чем больше, тем лучше. Практика показывает, что количество проекций может быть меньше этой величины при удовлетворительном качестве изображения. В практической работе регистрируют 60–64 проекции при сборе на матрицу 64×64 пиксела или 120–128 проекций при сборе на матрицу 128×128 пикселов за полный оборот детектора. При малом количестве проекций имеет место «эффект звезды». 4). Время регистрации одной проекции. С увеличением этого времени улучшается статистическая достоверность информации. При работе на однодетекторном томографе (при сборе на матрицу 64×64 пиксела) желательно, чтобы время сбора проекции не превышало 30 с — из расчета, время сбора всей информации не превысит 0–40 мин при регистрации 60–64 проекций. Более время исследования обременительно для больного. Кроме того, снижается пропускная способность томографа. Для уменьшения времени регистрации используют многодетекторные томографы и по возможности увеличивают активность РФП, вводимых пациенту. 5). Радиус ротации системы. Для получения качественного изображения радиус ротации должен быть минимальным. Разрешающая способность

повышается при движении детектора томографа по эллиптической или контурно-адаптированной
орбите. 6). Диапазон углов регистрации. Чаще всего проводят сбор информации за полный оборот детектора вокруг продольной оси тела пациента; при исследовании сердца сбор информации проводят при вращении детектора на угол 180°. 7). Режим сбора информации. Различают два
режима сбора информации: непрерывный и шаговый (режим step-shoot). При непрерывном режиме детектор двигается непрерывно по заданной орбите вокруг продольной оси тела пациента, собирая данные в режиме ротации. Затем данные обрабатываются при помощи компьютера с получением заданного количества проекций. При шаговом режиме по завершении сбора проекции детектор осуществляет поворот на определенный угол, и проводится сбор следующей проекции. Этот процесс повторяется до тех пор, пока не будет пройдена вся траектория. При непрерывном режиме сбора информации выше чувствительность, но хуже разрешающая способность, особенно при малом количестве проекций. При большом количестве проекций «эффект размазывания» изображений практически сводится к нулю. При шаговом режиме выше разрешающая способность, но ниже чувствительность, так как происходит затрата времени на перемещение де тектора между отдельными проекциями, который в эти промежутки времени не собирает диагностическую информацию. Но при этом режиме при сборе небольшого количества проекций отсутствует «эффект размазывания» изображений. 8). Тип коллиматора. Оптимальными являются коллиматоры высокого разрешения; допускается применение коллиматоров общего назначения. При применении коллиматоров высокого разрешения необходимо вводить более высокие активности РФП для сокращения времени исследования и обеспечения статистической достоверности информации. Факторы, влияющие на качество изображения: 1. Неоднородность поля зрения. Вариации
равномерности поля зрения, приемлемые для планарных исследований, могут быть источником
артефактов на реконструированных изображениях. Значительная неоднородность приводит к по-
явлению на реконструированных изображениях концентрических окружностей. Для избежания
этих артефактов применяют микропроцессорную систему коррекции неоднородности, а также создают матрицу коррекции неоднородности с радионуклидом, применяемым для проведения данного исследования. В процессе реконструкции коррекции подлежит каждая проекция, полученная на этапе сбора. 2. Положение центра ротации системы. При возникновении дрейфа центра ротации происходит размазывание изображения. При проверке координаты точечного источника должны совпадать с центром матрицы визуализации. После коррекции допускается смещение центра не более, чем на 0,5 пиксела. В некоторых современных томографах микропроцессоры осуществляют контроль центра ротации при сборе информации в реальном
масштабе времени. 3. Толщина срезов. Увеличение толщины срезов, выраженной в пикселах, способствует улучшению статистических характеристик изображения. Однако это приводит к потере пространственного разрешения и чувствительности при выявлении небольших неоднородностей. 4.Ослабление излучения (аттенюация). При прохождении фотонов через тело пациента про-
исходит их ослабление. Неоднородность ослабления излучения в теле пациента влияет не только
на точность количественного картирования пространственного распределения активности РФП,
Качество изображения в большой степени зависит от алгоритма реконструкции. Алгоритмы
реконструкции изображений подразделяются на две большие группы: аналитические алгоритмы
и итеративные алгоритмы. К первой группе относятся: алгоритмы обратного проецирования с фильтрацией и двумерная реконструкция по Фурье. Ко второй группе относятся: традиционные
алгоритмы — алгебраический метод восстановления (ART), метод одновременного итеративного
восстановления (SIRT) и итеративный метод наименьших квадратов (ILST) и т.д.
Однофотонная эмиссионная компьютерная томография ( ОФЭКТ или, реже, СПЭТ ) - это метод томографической визуализации ядерной медицины с использованием гамма-лучей . Это очень похоже на обычную плоскую визуализацию в ядерной медицине с использованием гамма-камеры (то есть сцинтиграфию ), но может предоставить истинную трехмерную информацию. Эта информация обычно представлена в виде срезов пациента, но при необходимости ее можно свободно переформатировать или изменять.
Этот метод требует доставки пациенту гамма-излучающего радиоизотопа ( радионуклида ), обычно путем инъекции в кровоток. Иногда радиоизотоп представляет собой простой растворимый растворенный ион, такой как изотоп галлия (III). Однако в большинстве случаев радиоизотоп-маркер присоединяется к определенному лиганду для создания радиолиганда , свойства которого связывают его с определенными типами тканей. Это сочетание позволяет переносить комбинацию лиганда и радиофармпрепарата и связывать ее с интересующим местом в организме, где концентрация лиганда видна с помощью гамма-камеры.
СОДЕРЖАНИЕ
Принципы

Вместо того, чтобы просто «сфотографировать анатомические структуры», сканирование SPECT отслеживает уровень биологической активности в каждом месте анализируемой трехмерной области. Выбросы радионуклида указывают на количество кровотока в капиллярах визуализируемых областей. Точно так же, как обычный рентгеновский снимок представляет собой 2-мерный (2-D) вид трехмерной структуры, изображение, полученное с помощью гамма-камеры, является 2-мерным видом 3-мерного распределения радионуклида .
ОФЭКТ-визуализация выполняется с помощью гамма-камеры для получения нескольких двумерных изображений (также называемых проекциями ) под разными углами. Затем используется компьютер для применения алгоритма томографической реконструкции к нескольким проекциям, что дает набор трехмерных данных. Затем этим набором данных можно манипулировать, чтобы показать тонкие срезы вдоль любой выбранной оси тела, аналогичные тем, которые получены с помощью других томографических методов, таких как магнитно-резонансная томография (МРТ), рентгеновская компьютерная томография ( рентгеновская компьютерная томография ) и позитронно-эмиссионная томография (ПЭТ).
ОФЭКТ похожа на ПЭТ в использовании радиоактивного индикаторного материала и обнаружении гамма-лучей. В отличие от ПЭТ, индикаторы, используемые в ОФЭКТ, испускают гамма-излучение, которое измеряется напрямую, тогда как индикаторы ПЭТ испускают позитроны, которые аннигилируют с электронами на расстоянии до нескольких миллиметров, вызывая испускание двух гамма-фотонов в противоположных направлениях. Сканер ПЭТ обнаруживает эти выбросы «совпадающими» во времени, что дает больше информации о локализации событий излучения и, следовательно, изображения с более высоким пространственным разрешением, чем ОФЭКТ (разрешение около 1 см). Сканирование ОФЭКТ значительно дешевле, чем сканирование ПЭТ, отчасти потому, что оно позволяет использовать более долгоживущие и более легко получаемые радиоизотопы, чем ПЭТ.
Поскольку получение ОФЭКТ очень похоже на получение изображений с помощью планарной гамма-камеры, можно использовать те же радиофармпрепараты . Если пациент обследуется с помощью другого типа сканирования ядерной медицины, но изображения не являются диагностическими, можно сразу перейти к ОФЭКТ, переместив пациента к прибору ОФЭКТ или даже просто перенастроив камеру для получения изображения ОФЭКТ. пока пациент остается на столе.
Для получения изображений SPECT гамма-камера вращается вокруг пациента. Прогнозы снимаются в определенных точках во время вращения, обычно каждые 3–6 градусов. В большинстве случаев для получения оптимальной реконструкции используется полное вращение на 360 градусов. Время, необходимое для получения каждого прогноза, также варьируется, но обычно 15–20 секунд. Это дает общее время сканирования 15–20 минут.
Гамма-камеры с несколькими головками могут ускорить получение. Например, двухголовая камера может использоваться с головками, разнесенными на 180 градусов друг от друга, что позволяет снимать две проекции одновременно, причем каждая головка требует поворота на 180 градусов. Также используются тройные камеры с шагом 120 градусов.
Захват со стробированием сердца возможен с помощью ОФЭКТ, так же как и с помощью методов плоской визуализации, таких как сканирование с несколькими стробами (MUGA). Запущенная электрокардиограммой (ЭКГ) для получения дифференциальной информации о сердце в различных частях его цикла, закрытая ОФЭКТ миокарда может использоваться для получения количественной информации о перфузии миокарда, толщине и сократимости миокарда во время различных частей сердечного цикла, а также также для расчета фракции выброса левого желудочка , ударного объема и сердечного выброса.
Заявление
ОФЭКТ можно использовать в дополнение к любому исследованию гамма-визуализации, где может оказаться полезным истинное трехмерное представление, например, при визуализации опухоли, инфекции ( лейкоцитов ), визуализации щитовидной железы или сцинтиграфии костей .
Поскольку ОФЭКТ обеспечивает точную локализацию в трехмерном пространстве, ее можно использовать для получения информации о локализованных функциях внутренних органов, например, функциональной визуализации сердца или головного мозга.
Визуализация перфузии миокарда
Визуализация перфузии миокарда (MPI) - это форма функциональной визуализации сердца, используемая для диагностики ишемической болезни сердца . Основной принцип заключается в том, что в условиях стресса больной миокард получает меньший кровоток, чем нормальный миокард. MPI - это один из нескольких видов сердечного стресс-теста .
Вводят специфический для сердца радиофармпрепарат, например 99m Tc- тетрофосмин (Myoview, GE healthcare), 99m Tc-сестамиби ( Cardiolite , Bristol-Myers Squibb) или хлорид таллия-201 . После этого частота сердечных сокращений увеличивается, чтобы вызвать стресс миокарда, либо упражнениями на беговой дорожке, либо фармакологически с аденозином , добутамином или дипиридамолом ( аминофиллин может быть использован для отмены эффектов дипиридамола).
Визуализация SPECT, выполненная после стресса, показывает распределение радиофармпрепарата и, следовательно, относительный кровоток в различных областях миокарда. Диагностика проводится путем сравнения стрессовых изображений с дополнительным набором изображений, полученных в состоянии покоя, которые обычно получают до стрессовых изображений.
Было продемонстрировано, что общая точность MPI составляет около 83% ( чувствительность : 85%; специфичность : 72%) (в обзоре не только SPECT MPI) и сопоставима с другими неинвазивными тестами (или лучше) при ишемической болезни сердца.
Функциональная визуализация головного мозга
Обычно гамма-излучающий индикатор, используемый при функциональной визуализации мозга, представляет собой экзаметазим технеция (99mTc) . 99m Tc - это метастабильный ядерный изомер, который испускает гамма-лучи, обнаруживаемые с помощью гамма-камеры. Присоединение его к экзаметазиму позволяет ему поглощаться тканями мозга пропорционально мозговому кровотоку, что, в свою очередь, позволяет оценить церебральный кровоток с помощью ядерной гамма-камеры.
Поскольку кровоток в головном мозге тесно связан с локальным метаболизмом мозга и потреблением энергии, индикатор 99m Tc-экзаметазим (а также аналогичный индикатор 99m Tc-EC) используется для региональной оценки метаболизма мозга в попытке диагностировать и дифференцировать различные причинные патологии деменции . Мета-анализ многих опубликованных исследований показывает, что чувствительность ОФЭКТ с этим индикатором составляет около 74% при диагностике болезни Альцгеймера по сравнению с чувствительностью 81% при клиническом обследовании ( когнитивное тестирование и т. Д.). Более поздние исследования показали, что точность ОФЭКТ в диагностике болезни Альцгеймера может достигать 88%. В метаанализе ОФЭКТ превзошла клиническое обследование и клинические критерии (91% против 70%) в способности дифференцировать болезнь Альцгеймера от сосудистой деменции. Эта последняя способность связана с визуализацией локального метаболизма головного мозга с помощью ОФЭКТ, при которой точечная потеря коркового метаболизма, наблюдаемая при множественных инсультах, явно отличается от более равномерной или «плавной» потери не затылочной корковой функции мозга, типичной для болезни Альцгеймера. Другая недавняя обзорная статья показала, что многоголовые ОФЭКТ-камеры с количественным анализом дают общую чувствительность 84-89% и общую специфичность 83-89% в поперечных исследованиях, чувствительность 82-96% и специфичность 83-89. % для продольных исследований деменции.
ОФЭКТ-сканирование 99m Tc-экзаметазимом конкурирует с ПЭТ- сканированием на основе флудезоксиглюкозы (ФДГ) головного мозга, которое позволяет оценить региональный метаболизм глюкозы в головном мозге и предоставить очень похожую информацию о локальном повреждении мозга в результате многих процессов. ОФЭКТ более широко доступна, потому что используемый радиоизотоп является более долговечным и гораздо менее дорогостоящим в ОФЭКТ, а также менее дорогое оборудование для гамма-сканирования. В то время как 99m Tc извлекается из относительно простых генераторов технеция-99m , которые еженедельно доставляются в больницы и сканирующие центры для снабжения свежим радиоизотопом, FDG PET полагается на FDG, который производится на дорогостоящем медицинском циклотроне и в «горячей лаборатории» (автоматизированная химия). лаборатории для производства радиофармпрепаратов), а затем немедленно доставили в места сканирования из-за естественного короткого периода полураспада фтора-18, составляющего 110 минут .
Применения в ядерной технологии
В ядерной энергетике метод SPECT может применяться для визуализации распределения радиоизотопов в облученном ядерном топливе. Из-за облучения ядерного топлива (например, урана) нейтронами в ядерном реакторе в топливе естественным образом образуется широкий спектр гамма-излучающих радионуклидов, таких как продукты деления ( цезий-137 , барий-140 и европий-154 ). и продукты активации ( хром-51 и кобальт-58 ). Их можно визуализировать с помощью ОФЭКТ для проверки наличия топливных стержней в хранимой топливной сборке для целей гарантий МАГАТЭ , для проверки прогнозов кодов моделирования активной зоны или для изучения поведения ядерного топлива при нормальной эксплуатации или в аварийных сценариях. .
Реконструкция

Восстановленные изображения обычно имеют разрешение 64 × 64 или 128 × 128 пикселей с размером пикселей в диапазоне 3–6 мм. Количество полученных проекций выбирается примерно равным ширине получаемых изображений. Как правило, полученные восстановленные изображения будут иметь более низкое разрешение, будут иметь повышенный шум, чем плоские изображения, и будут подвержены артефактам .
Сканирование занимает много времени, и очень важно, чтобы во время сканирования пациент не двигался. Движение может вызвать значительное ухудшение восстановленных изображений, хотя методы восстановления с компенсацией движения могут помочь в этом. Крайне неравномерное распределение радиофармпрепарата также может вызвать артефакты. Область очень интенсивной активности (например, мочевой пузырь) может вызвать появление обширных полос на изображении и затемнить соседние области активности. Это ограничение алгоритма реконструкции отфильтрованной обратной проекции . Итеративная реконструкция - это альтернативный алгоритм, важность которого возрастает, поскольку он менее чувствителен к артефактам и может также корректировать затухание и размытие, зависящее от глубины. Кроме того, итерационные алгоритмы могут быть сделаны более эффективным использованием Superiorization методологии.
Рассеяние гамма-лучей, а также случайный характер гамма-лучей также могут привести к ухудшению качества изображений SPECT и вызвать потерю разрешения. Коррекция рассеяния и восстановление разрешения также применяются для улучшения разрешения изображений SPECT.
Типичные протоколы получения ОФЭКТ
| Изучение | Радиоизотоп | Энергия излучения (кэВ) | Период полураспада | Радиофармпрепараты | Активность ( МБк ) | Вращение (градусы) | Прогнозы | Разрешение изображения | Время на проекцию (с) |
|---|---|---|---|---|---|---|---|---|---|
| Рентген | технеций-99m | 140 | 6 часов | Фосфонаты / бисфосфонаты | 800 | 360 | 120 | 128 х 128 | 30 |
| Сканирование перфузии миокарда | технеций-99m | 140 | 6 часов | тетрофосмин; Сестамиби | 700 | 180 | 60 | 64 х 64 | 25 |
| Сканирование паращитовидных желез Sestamibi | технеций-99m | 140 | 6 часов | Сестамиби | |||||
| Сканирование мозга | технеций-99m | 140 | 6 часов | Tc exametazime; ECD | 555-1110 | 360 | 64 | 128 х 128 | 30 |
| Нейроэндокринное или неврологическое сканирование опухолей | йод-123 или йод-131 | 159 | 13 часов или 8 дней | MIBG | 400 | 360 | 60 | 64 х 64 | 30 |
| Сканирование белых клеток | индий-111 и технеций-99m | 171 и 245 | 67 часов | лейкоциты, меченные in vitro | 18 | 360 | 60 | 64 х 64 | 30 |
ОФЭКТ / КТ
В некоторых случаях гамма-сканер SPECT может быть построен для работы с обычным компьютерным томографом с одновременной регистрацией изображений. Как и в ПЭТ / КТ , это позволяет определять местонахождение опухолей или тканей, которые можно увидеть на сцинтиграфии ОФЭКТ, но которые трудно определить точно относительно других анатомических структур. Такое сканирование наиболее полезно для тканей за пределами головного мозга, где расположение тканей может быть гораздо более изменчивым. Например, ОФЭКТ / КТ может использоваться в приложениях сканирования паращитовидных желез сестамиби , где этот метод полезен для обнаружения эктопических аденом паращитовидных желез, которые могут находиться не на своих обычных местах в щитовидной железе.
Контроль качества
Общие характеристики систем SPECT могут быть выполнены с помощью инструментов контроля качества, таких как фантом Ящака .
Термин «эмиссионная томография» (ЭТ) относится к двум методам получения трехмерных изображений областей интереса. Обе техники основаны на внедрении в организм пациента РФП и измерении радиационного поля, создаваемого излучением радионуклида вне тела больного. К ЭТ относится однофотонная эмиссионная компьютерная томография (ОФЭКТ) и двухфотонная эмиссионная компьютерная томография (позитронная эмиссионная томография, ПЭТ). Оба метода применяются для исследования биологических функций в организме человека с целью обнаружения и описания отклонений, характерных для конкретных заболеваний — онкологических, неврологических, сердечно-сосудистых и т.п.
Эмиссионная компьютерная томография, как и сцинти- графия, генерирует «молекулярные» изображения, создаваемые излучением от молекул РФП, распределенных в организме человека. Метод является неинвазивным, т.е. никак не повреждает исследуемый объект.
Основными стадиями эмиссионной томографии являются: производство РФП, введение РФП в тело пациента, сбор данных, измерение у-излучения, реконструкция и анализ изображения.
Эмиссионная томография позволяет визуализировать протекание биологических процессов in vivo. Она реализуется путем интеграции двух методик: кинетического варианта метода меченых атомов и компьютерной томографии. Анализ кинетики накопления и выведения молекулярного зонда, в качестве которого используется меченное радионуклидом биологически активное вещество, проводится в рамках математических моделей, описывающих динамику перераспределения РФП при его вовлечении в биологический процесс. Томография дает возможность преобразовать невидимые поперечные сечения через внутренности человека в видимые изображения, доступные для анализа на компьютере. Технология позволяет обращаться с изображением как с массивом чисел, представляющих локальные значения свойств изучаемого объекта, а также рассчитывать необходимые для диагноза параметры органов и тканей. Результатом являются трехмерные изображения анатомических распределений РФП, возникающие в ходе протекания исследуемого биологического процесса.
В ходе эмиссионной томографии проводится регистрация излучения, накопление данных, их предварительная обработка, построение изображений, их восстановление, анализ, интерпретация и постановка диагноза. Формирование изображений означает не только отображение свойств объекта на поверхность проекции этого изображения, но и классификацию объектов по их физическим, химическим и радиологическим свойствам. Сюда входят стратегии отображения, математические концепции, используемые для моделирования этих стратегий, классификация недостатков, характерных для конкретных типов отображения. Проводится определение границ зон интереса, измеряется периметр, площадь и объем объекта, характеризуется его сегментация, текстура, описывается характер движения диагностируемого объекта. Процесс заканчивается морфологическим анализом изображения и оценкой точности диагностики.
В эмиссионной томографии данные записываются прибором, создающим изображение, и представляются в форме проекций. Цель томографии — оценка распределения РФП по некоторому срезу, исходя из проекционных данных. В системах ЭТ получают проекции для множества различных одномерных срезов одновременно, после чего создается трехмерное (3D) распределение радиоактивного вещества.
Первой стадией томографии является производство РФП, подходящего для обнаружения заболевания. Качество изображения зависит от количества введенного в исследуемый объект РФП, однако действие излучения на внутренние органы накладывает ограничения на размер безопасной дозы препарата. Молекулы РФП метят у-излучающим радионуклидом. Радиация распространяется во всех направлениях изнутри тела пациента с интенсивностью, пропорциональной локальной концентрации РФП (эта концентрация зависит от способности изучаемого объекта аккумулировать РФП, причем важно, чтобы концентрация метки в диагностируемом органе была существенно выше, чем в окружающих тканях). Гамма-лучи, исходящие от пациента, детектируются и записываются в память компьютера. Детекторы окружают пациента или вращаются вокруг него. Регистрируется интенсивность излучения в различных направлениях выхода у-лучей, а затем результаты оцифровываются и преобразуются в гистограмму из столбцов, содержащих параметры проекций.
При статическом исследовании на изображениях фиксируется распределение РФП в среднестатистический момент времени относительно всего периода получения данных. Такое исследование возможно, когда физиологически обусловленные изменения в распределении РФП во времени очень медленные или когда количество испускаемых у-лучей настолько мало, что для создания изображения с удовлетворительным качеством требуется длительный период получения данных.
Динамическое исследование имеет цель зафиксировать распределение РФП как функцию времени. Такое исследование применятся для визуальной оценки функции органа. Оно необходимо для определения кинетических параметров. В импульсном исследовании получение данных синхронизировано с ритмом сердечных сокращений или с дыханием пациента. Важное применение метода — исследование деятельности сердца, представленное в виде короткого фильма, передающего движение во время одного сердечного цикла пациента. Этот единственный удар сердца является сложной картиной, сформированной с помощью усреднения данных, собранных за время наблюдения большого количества сердечных циклов. При импульсной томографии сердца сигнал электрокардиограммы используется для синхронизации полученных данных. Гамма-лучи, регистрируемые сразу же после начала каждого сердечного цикла, объединяются для формирования составного первого кадра.
ПЭТ и ОФЭКТ различаются по типу радиоизотопа, являющегося меткой: в ОФЭКТ-исследованиях используются РФП, меченные изотопом, являющимся источником у-излу- чения, а в ПЭТ — р + -излучения.
Однофотонная эмиссионная компьютерная томография (ОФЭКТ) позволяет получать объемное изображение распределения у-излучающих радионуклидов. Схема диагностики приведена на рис. 7.8.
В этом методе на основе 2.0-изображений срезов тканей (органов) с помощью компьютерных программ реконструируют трехмерное изображение. Для достижения высокого качества сканирования энергия у-кванта должна составлять 60—300 кэВ. В этом случае основные радионуклиды для однофотонной томографии — это ""'Тс, 131 1, 123 1, 111 In и др. (табл. 7.2). Как правило, они же применяются для сцинтиграфии.
Специфические РФП, проникающие в опухолевые клетки, включаются в метаболизм опухолей. К ним относятся изотопы йода 123 1 и 131 1, [ 123 1]-метайод-бензил-шуаиидин ([ 123 1)-МИБГ) и пятивалентный [ 99 '"Тс(У)]-ДМСА. Иод-131 успешно используется для диагностики различных видов рака щитовидной железы и его метастазов. Дифференцированные опухоли щитовидной железы сохраняют способность захватывать йод и включать его в синтез тиреоидных гормонов. Раковая опухоль в таких случаях визуализуется в виде «го-

Рис. 7.8. Схема метода однофотонной эмиссионной томографии
Радионуклидная диагностика – раздел ядерной медицины, основанный на выявлении болезней с помощью радиоактивных меток или радиофармпрепаратов. Метод основан на принципе меченых атомов, согласно которому, радиоактивные вещества принимают такое же участие в процессах жизни клетки, как и не радиоактивные. Поэтому изучая распределение радиоактивной метки в организме больного с помощью специальных детектирующих аппаратов, например таких как ОФЭКТ-КТ и ПЭТ-КТ , врач получает возможность увидеть самые начальные проявления опухоли
Как проходит исследование? Пациенту внутривенно вводят радиоактивный препарат, и врач через определенное время с помощью современного оборудования (ОФЭКТ-КТ или ПЭТ-КТ) видит его пространственное распределение в клетках, тканях или органах у обследуемого человека. С помощью современных компьютерных систем формируется изображение, которое анализируют обычно не менее 2 специалистов.

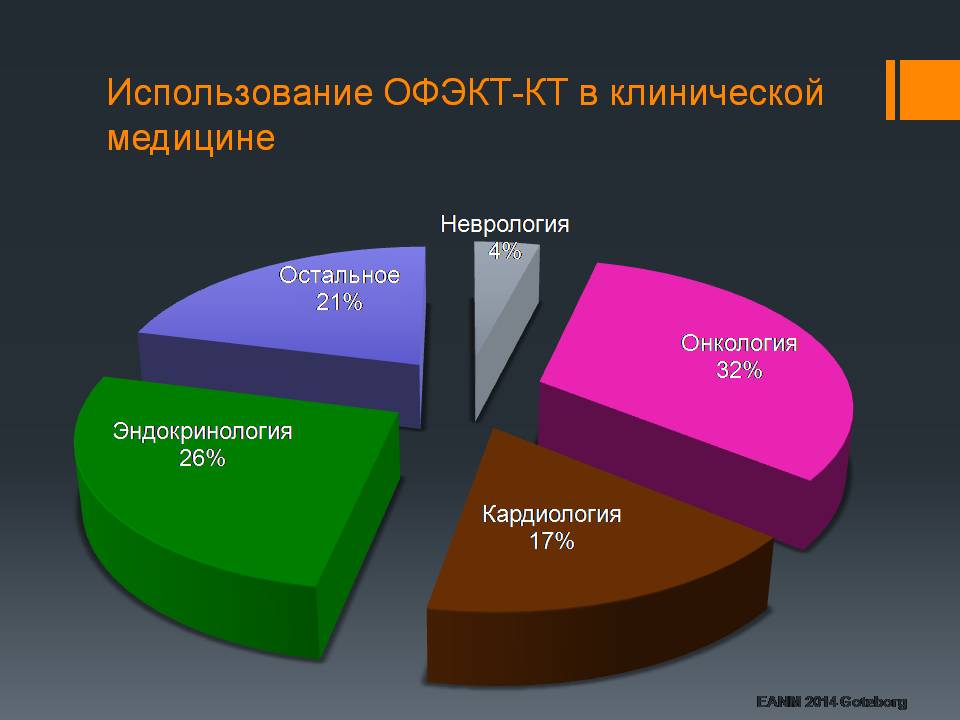
По данным Европейского общества ядерной медицины, треть всех ОФЭКТ-КТ исследований производится в онкологии.
С помощью ОФЭКТ-КТ исследования мы можем определить аномально протекающие биохимические процессы в опухолевых клетках, когда анатомические и морфологические изменения еще не видны и не могут быть выявлены с помощью методов классической лучевой диагностики, таких, как рентгенография или КТ. С помощью методов радионуклидной диагностики сегодня мы можем диагностировать опухоли размерами менее 1 сантиметра.
Главная задача радионуклидных исследований в онкологии – оценка распространенности опухолевого процесса и оценка эффективности лечения.
Основные методы лучевой и радионуклидной диагностики разделяют на две категории
- Рентгенография
- Компьютерная томография (КТ)
- Магнитно-резонансная томография (МРТ)
- Сцинтиграфия
- Однофотонная эмиссионная компьютерная томография (ОФЭКТ)
- Позитронно-эмиссионная томография (ПЭТ)
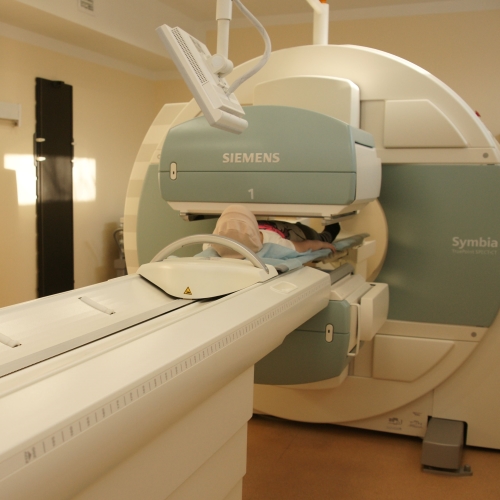
Гибридные методы сочетают в себе анатомические и функциональные. К ним относится ОФЭКТ-КТ и ПЭТ-КТ. В отделении радионуклидной диагностики НМИЦ онкологии им. Н.Н. Петрова установлен гибридный аппарат «SiemensSymbiaT16». Этот прибор сочетает в себе двухдетекторную гамма-камеру и 16-срезовый компьютерный томограф. В целом информативность ОФЭКТ-КТ выше, чем КТ + ОФЭКТ отдельно. Исследования достаточно безопасны для пациентов.

За одно обследование получается максимум диагностической информации. Например, при раке молочной железы на ОФЭКТ-КТ томографе Siemens за одно исследование мы можем оценить состояние молочной железы, регионарных лимфатических узлов, органов грудной и брюшной полостей. В результате, пациент может начать специфическое противоопухолевое лечение максимально быстро.
Преимущества ОФЭКТ-КТ
- Позволяет получить трехмерное функциональное изображение
- Высокое качество изображения
- Возможность точной анатомической локализации выявленный патофизиологических процессов
- Возможность одновременной совместной оценки выявленных функциональных и структурных нарушений
Диагностика метастатического поражения скелета
Наибольшее распространение этот метод получил в исследовании костей. ОФЭКТ-КТ исследование объединяет преимущества остеосцинтиграфии – высокую чувствительность и рентгенографии – высокую специфичность.

В результате ОФЭКТ-КТдиагностики могут быть выявлены новые уточняющие данные и даже может измениться диагноз. По опыту отделения радионуклидной диагностики НМИЦ онкологии им. Н.Н. Петрова: после рутинной остеосцинтиграфии в 40% случаев изменялся диагноз.
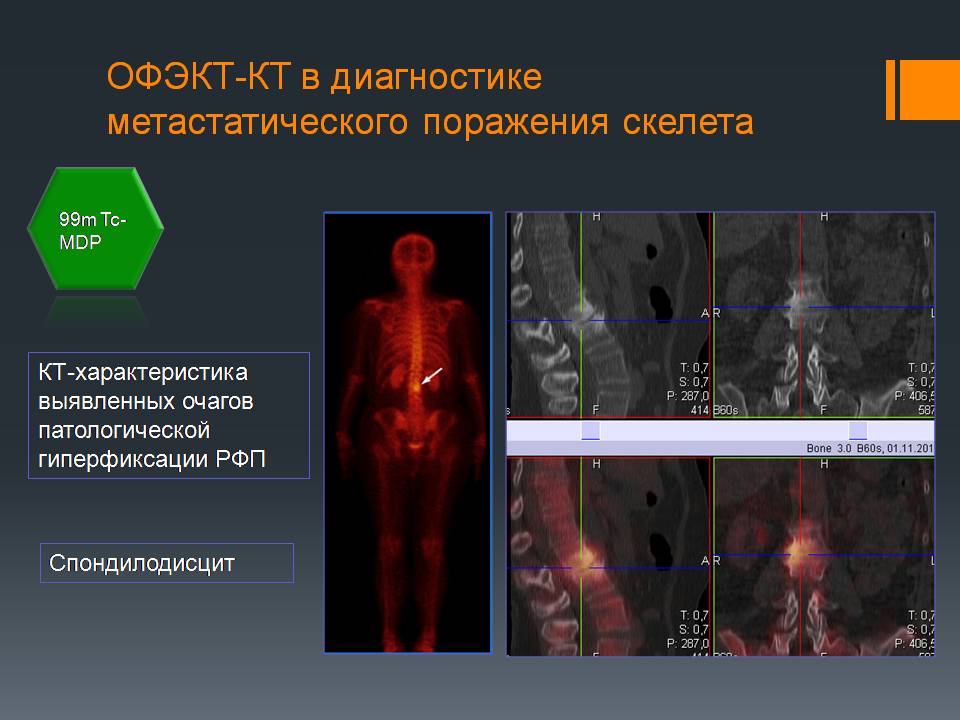
Пример уточняющей диагностики: При КТ-исследовании выявлен очаг, подозрительный на метастазы в 3 поясничном позвонке. После выполнения ОФЭКТ-КТ видно, что это спондилодисцит позвоночника, не онкологическое заболевание.
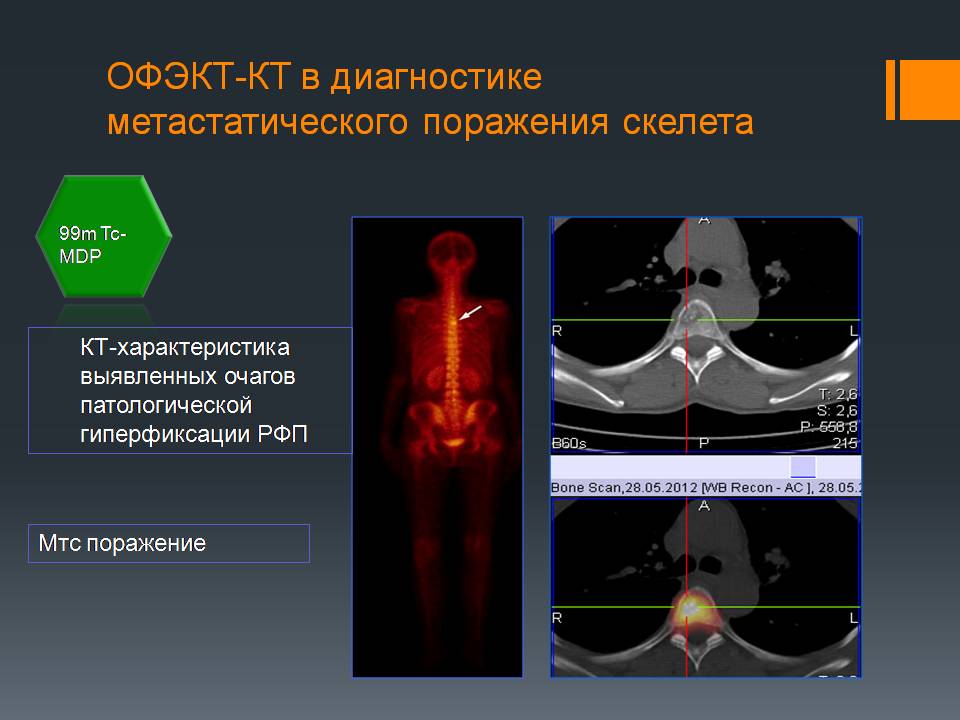
Пример уточняющей диагностики: Выявлен очаг гиперфиксации подозрительный на мтс. На снимке ОФЭКТ-КТ подтверждается, что это метастазы.
Диагностика метастатического поражения регионарных лимфоузлов у больных РМЖ
Статус регионарных лимфатических узлов влияет не только на прогноз, но и на выбор лечебной тактики, на объем лучевой терапии. При поражении лимфоузлов лучевая терапия может проводиться в над- и подключичной области. А при отсутствии метастазов облучается только грудная стенка и даже возможно полное отсутствие лучевой терапии.
Биопсия сигнальных лимфоузлов у больных РМЖ
Современное лечение РМЖ немыслимо без методов радионуклидной диаг ностики. Известно, что состояние сигнального лимфоузла определяет состояние всех остальных лимфоузлов. При помощи ОФЭКТ-КТ можно анатомически точно определить сигнальный лимфоузел. Во-первых, это помощь для хирурга: точная локализация позволяет ему быстрее обнаружить нужный лимфоузел. Во-вторых, результат исследования облегчает навигацию при последующей лучевой терапии.
ОФЭКТ-КТ также успешно применяется в диагностике нейроэндокринных новообразований, в диагностике метастазов при раке предстательной железы.

Авторская публикация:
Крживицкий Павел Иванович
врач-рентгенолог, врач-радиолог, кандидат медицинских наук.
Заведующий отделением радионуклидной диагностики, cтарший научный сотрудник отдела ядерной медицины и радиационной онкологии

В диагностическом багаже врачей имеются рентгенография, компьютерная томография (КТ), магнитно-резонансная томография (МРТ), ультразвуковая диагностика (УЗД), радиоизотопные методики, такие как позитронно-эмиссионная томография (ПЭТ) и однофотонная эмиссионная компьютерная томография (ОФЭКТ). Технический прогресс позволил внести огромные изменения в технологии получения изображений. Благодаря этим инновациям значительно возросли диагностические возможности современных приборов. Важную роль стали играть комбинированные системы. Подобные устройства сочетают в себе все достоинства современных томографических методов. Это единые компактные и интегрированные системы, позволяющие выполнять исследования различных типов.
В ФГБУ «Клиническая больница №1» установлена современная комбинированная система ОФЭКТ/КТ SYMBIA T16 фирмы Siemens, сочетающий в себе преимущества гамма-камеры и мощность 16-ти срезового КТ-сканера, что позволило поднять диагностический процесс на совершенно новый качественный уровень.
ОФЭКТ/КТ - технология, органично сочетающая в себе функциональную чувствительность ОФЭКТ с высокой анатомической детализацией многослойной КТ. Подобное сочетание обеспечивает отличное качество изображений, позволяющее точно локализовать очаги поражения. ОФЭКТ/КТ обеспечивает одновременное получение диагностической информации для обоих типов исследований. Это приводит к повышению точности обоих типов исследования. Благодаря этому врачи могут делать выводы куда увереннее, чем раньше. Точное совмещение анатомических и функциональных изображений повышает надежность определения и локализации очагов поражения.
Благодаря возможности выполнения двух оптимизированных сканов в ходе исследования, ОФЭКТ/КТ поднимает эффективность работы на непревзойденный уровень, позволяя при этом получать изображения самого высокого качества. Применение этой методики в онкологии позволяет достовернее определять наличие или отсутствие заболевания, а также степень его выраженности. Добавление многослойной КТ дает возможность получать ценную анатомическую информацию, необходимую для точной локализации патологического процесса.
ОФЭКТ/КТ идеально подходит для задач, связанных с визуализацией опухолей, например, для исследований пациентов с метастатическим раком молочной или предстательной железы, первичным раком кости, нейроэндокринными опухолями, аденомами паращитовидной железы, невромами, нейробластомами, множественными миеломами или раком печени. (Рис. 1)
В дополнение к этому данные КТ позволяют делать коррекцию на ослабление излучения тканями, благодаря чему становится возможным количественный анализ результатов ОФЭКТ. Количественная оценка накопления радиофармпрепарата при проведении ОФЭКТ способствует совершенствованию методов стадирования опухоли и планирования терапевтических процедур.
Интеграция ОФЭКТ с КТ предоставляет врачам новые возможности для оценки риска заболеваний коронарных артерий. Эта новая технология дает возможность количественно оценить кальцификацию коронарных артерий, определить проходимость сосудов и измерить перфузию и жизнеспособность миокарда с помощью единой комбинированной системы. Недавние научные исследования и бурное развитие компьютерной томографии сердца и сосудов продемонстрировали огромный потенциал этого метода. Благодаря полностью интегрированной системе многослойной КТ получается подробная карта ослабления излучения, при этом время сканирования увеличивается не более чем на 30 секунд. Данный метод гарантирует точную коррекцию эмиссионных изображений и соответствующее повышение их качества. Совместный просмотр результатов исследования, полученных одновременно с помощью дополняющих друг друга средств визуализации, увеличивает достоверность диагностики. (Рис. 2)
ОФЭКТ является высокоинформативным методом функциональной нейровизуализации и обладает высоким диагностическим потенциалом при ряде неврологических заболеваний. Этот вид исследования головного мозга обладает высокой информативностью при дифференциальной диагностике различных видов деменций в нейропсихиатрической практике; при эпилепсии, нейротравмах, нейродегенеративных и некоторых наследственных заболеваниях головного мозга. ОФЭКТ головного мозга позволяет получить трехмерное изображение перфузии и метаболического статуса ткани головного мозга. Благодаря возможности прямой визуализации мозговой перфузии, ОФЭКТ является одним из ведущих методов исследования при сосудистых заболеваниях головного мозга, при помощи которого эффективно распознаются ранние стадии мозговой ишемии. Кроме того, доказано, что уровень перфузии головного мозга прямо пропорционален уровню его метаболизма.
Полученная информация зачастую дополняет данные о структурно-морфологических изменениях ткани головного мозга, полученных при компьютерно-томографическом исследовании, которые могут быть получены сразу интегрированным в комбинированный аппарат КТ сканером. Кроме того, при ОФЭКТ/КТ получается точное картирование головного мозга и анатомическая привязка выявленных зон нарушения перфузии, что также повышает диагностическую значимость метода. (Рис. 3 а, б)
В настоящее время идет разработка большого количества специфичных к различным опухолям радиофармпрепаратов для ОФЭКТ и специализированных агентов для радионуклидной терапии. Опухоли, к которым применяются данные препараты, невозможно обнаружить с помощью других диагностических методов. Чем выше специфичность препаратов, тем сильнее ощущается необходимость в непосредственном получении точной анатомической информации. Благодаря полной интеграции и исключительному качеству изображений ОФЭКТ/КТ идеально подходит для эффективной визуализации специализированных радиофармпрепаратов и агентов, что позволяет врачам точно локализовать полученную функциональную информацию.
Читайте также:


